Artigo original
DESENVOLVIMENTO E VALIDAÇÃO DE MÉTODO ANALÍTICO PARA QUANTIFICAÇÃO DO TEOR DE FORMALDEÍDO POR HPLC EM LEITE
Development and validation of an analytical method for quantification of formaldehyde content by HPLC in milk
https://doi.org/10.18593/evid.32593
Recebido em 15 de março de 2023 | Aceito em 17 de maio de 2023
Ana Carolina de Souza Canário* Natália Neto Pereira Cerize†
Natália Neto Pereira Cerize† Amanda Marcante‡
Amanda Marcante‡
Ana Paula Nunes de Sá§
 Veridiana Petenati da Rovare¶
Veridiana Petenati da Rovare¶ Wesley Feliciano dos Santos**
Wesley Feliciano dos Santos**
Sandra Souza de Oliveira††
Resumo:
O leite é um alimento constantemente sujeito a fraudes, sendo as mais frequentes a adição de água, reconstituintes e conservantes como formaldeído (FA), utilizado para inibir o crescimento microbiano, aumentando a vida útil do produto. À medida que novas técnicas de adulteração surgem, novos métodos para detecção de fraudes devem ser desenvolvidos, com a finalidade de manter a qualidade e a autenticidade do leite. O presente trabalho tem como objetivo desenvolver e validar um método com sensibilidade de detecção de traços e uma boa capacidade em resistir a pequenas variações, com intuito de quantificar FA em leite, empregando a técnica de extração líquido-líquido, juntamente com método de cromatografia líquida de alta eficiência com detecção por arranjo de diodos (CLAE-DAD) no comprimento de onda de 360 nm. Para a validação do método aplicou-se os parâmetros analíticos de linearidade, seletividade, especificidade, precisão, exatidão, limite de detecção (LDM), quantificação do método (LQM) e, robustez. O método demonstrou ser linear na faixa de trabalho de 0,03 a 0,1 mg/L, LDM e LQM de 0,004 mg/kg e 0,01 mg/kg, respectivamente. A exatidão avaliada, apresentou na faixa de 88% a 110% de recuperação. A precisão apresentou coeficiente de variação (CV) na faixa de 1% a 4% demonstrando ser seletivo, preciso e exato. Traços de formaldeídos foi encontrada em apenas uma amostra com valor acima do LQ onde a concentração encontrada de DNPH-FA foi de 0,028 mg/kg com recuperação de 93%. Assim podendo concluir que o método foi eficaz e poderá contribuir para a segurança alimentar.
Palavras-chave: Formaldeído. CLAE-DAD. Leite. ANVISA. Validação analítica.
Abstract:
Milk is a food constantly subject to fraud, the most frequent being the addition of water, restoratives and preservatives such as formaldehyde (FA), used to inhibit microbial growth, increasing the shelf life of the product. As new adulteration techniques emerge, new fraud detection methods must be developed in order to maintain the quality and authenticity of the milk. The present work aims to develop and validate a method with trace detection sensitivity and a good ability to resist small variations, in order to quantify FA in milk, using the liquid-liquid extraction technique, together with the liquid chromatography method high-efficiency detector with diode array detection (HPLC-DAD) at a wavelength of 360 nm. For method validation, the analytical parameters of linearity, selectivity, specificity, precision, accuracy, detection limit (LDM), method quantification (LQM) and robustness were applied. The method proved to be linear in the working range of 0.03 to 0.1 mg/L, LDM and LQM of 0.004 mg/kg and 0.01 mg/kg, respectively. The evaluated accuracy presented in the range of 88% to 110% of recovery. Precision showed a coefficient of variation (CV) in the range of 1% to 4%, demonstrating to be selective, precise and accurate. Traces of formaldehyde were found in only one sample with a value above the LQ where the concentration found for DNPH-FA was 0.028 mg/kg with a recovery of 93%. Thus, it can be concluded that the method was effective and could contribute to food security.
Keywords: Formaldehyde. CLAE-DAD. Milk. ANVISA. Analytical Validation.
@Autor correspondente: Mestre em Vigilância Sanitária. Autor correspondente. Laboratório de Químicas Manufaturados – LQM-IPT, CEP 05508-901, São Paulo/SP; https://orcid.org/0000-0002-5265-4562; anapaulasa@ipt.br.
1 INTRODUÇÃO
O leite está presente na dieta humana ao longo de toda sua vida, por ser uma fonte nutricional de alto valor biológico: proteína, minerais, vitaminas, carboidratos e lipídios1-2. Na produção, seu cenário em 2022 apresentou 21.560.569 milhões litros de leite cru adquirido e 21.483.602 milhões litros industrializado no Brasil, segundo o Instituto Brasileiro de Geografia e Estatística (IBGE)3. Nos três anos anteriores o mercado do leite apresentou um período de menor volume de produção, decorrente do período sazonal e disponibilidade de alimentação dos animais, visto que seu atual panorama de 2023 segundo a Companhia Nacional de Abastecimento (CONAB)4 expõem um ótimo cenário nesses três meses. Esse impacto da produção leiteira gera consequentemente a busca por suprir a demanda, aumentando o risco de fraudes no leite5.
Neste contexto, há dez anos, os laticínios do estado do Rio Grande do Sul, passava pela primeira apuração de adulteração no leite, nomeada de “Operação Leite Compensado” criada pelo Ministério da Agricultura, Pecuária e Abastecimento (MAPA), juntamente com o Ministério Público do Rio Grande do Sul (MP-RS), a investigação apontava uma fraudulenta adição de uréia agrícola em leite cru, com objetivo de aumentar o volume com água e manter os padrões de identidade das proteínas do leite. Essa uréia adicionada ainda apresentava em sua composição, formaldeído (FA) considerado um agente carcinogênico6-7.
A complexidade da via de contaminação química fraudulenta do leite está associada de forma lucrativa, aumento da vida de prateleira, melhorar/elevar teor nutricional ou até mesmo para mascarar algo estranho no leite. A capacidade dos adulterantes no leite tem ação direta na qualidade e indiretamente na saúde, o formaldeído (FA) por exemplo se liga nas cadeias de proteínas e lipídios e tem um efeito cumulativo, alojando diretamente no fígado ou até mesmos rapidamente absorvido no trato respiratório e gastrointestinal8-10.
Segundo um levantamento bibliográfico Oliveira et al.11, o leite é classificado como um dos alimentos suscetível a adulteração, a presença do (FA) em alguns países como na Índia é legalmente permitida para preservação de leite destinado a análises químicas em um nível de 0,4% (v/v) de leite. A autoridade Europeia para a Segurança dos Alimentos (EFSA), concede uma exposição diária ao (FA) proveniente de alimentos de origem animal e vegetal não deve exceder 100 mg/kg de alimento por dia12-13.
Hoje as plataformas brasileiras de recepção e nas indústrias de produtos lácteos o método praticado para determinação de formaldeído em leite está descrito na Instrução Normativa MAPA Nº 68/200614 e prevê apenas um teste colorimétrico qualitativo, que reporta “positivo” caso haja presença de formaldeído e “negativo” em caso contrário, método B da norma AOAC 931.0815 que impede que os métodos analíticos e os resultados obtidos sejam conclusivos e façam distinção entre origem endógena (produzida no interior de um organismo) ou adição fraudulenta de (FA), quando a faixa de concentração baixa é encontrada no leite.
Contudo, à medida que novas técnicas e substâncias fraudulentas contendo formaldeídos (FA) vão surgindo, novos métodos para detecção do adulterante vão sendo desenvolvidos com a finalidade de manter a qualidade e/ou autenticidade do leite16-19. Com intuito de apoiar as autoridades reguladoras, o presente estudo teve como objetivo desenvolver, otimizar e validar um método com sensibilidade de detecção e técnica de análise robusta utilizando cromatografia Líquida de Alta Eficiência com Detecção por Arranjo de Diodos (CLAE/DAD) para identificar e quantificar traços de (FA) em leite cru e derivados.
2 MATERIAIS E MÉTODOS
2.1 PADRÕES E REAGENTES
Materiais de referência certificados de formaldeído na concentração de 1000 μg/mL em água foram adquiridos da Sigma-Aldrich (St. Louis, EUA) e AccuStandard (New Haven, EUA). Acetonitrila grau HPLC da J.T. Baker (Phillipsburg, EUA), água ultrapura obtida de um sistema de purificação Milli-Q® Advantage A10 (Billerica, EUA), ácido fosfórico 85% P.A. da Merck (Darmstadt, Alemanha), e 2,4-dinitrofenilhidrazina (DNPH) derivatizante grau HPLC da Fluka (Morris Plains, EUA) foram utilizados para o preparo das amostras e fase móvel (FM).
Foram preparadas soluções de trabalho de (FA) na concentração de 2 mg/L em água para obtenção das curvas analíticas e fortificações, e solução de DNPH a 3 mg/mL em água e acetonitrila 40:60 (v/v) acidificada com 100 μL de ácido fósfórico 85%, de modo a alcançar pH igual a 3,0, para a derivatização do analito.
2.2 AMOSTRAS
Leite UHT integral bovino foi utilizado como branco de amostra no desenvolvimento e validação do método. Para a aplicação em amostras reais, quinze amostras de leite de diferentes tipos e marcas comerciais foram adquiridas em supermercados da cidade de São Paulo, SP, a saber: leite UHT integral (5), leite UHT semi-desnatado (4), leite UHT desnatado (4), e leite UHT sem lactose (2).
A molécula de FA possui alta volatilidade e polaridade, e baixa aborção na região do UV-Vis, dificultando sua retenção em colunas de fase reversa e detecção direta pelos detectores comumente utilizados em cromatografia líquida e gasosa20-21, de modo que sua derivatização se faz necessária. A principal reação de derivatização utilizada na análise de FA por CLAE-DAD é a adição nucleofílica de 2,4-dinitrofenilhidrazina (DNPH) em meio ácido (figura 1a)22. O produto colorido da reação, a 2,4-dinitrofenilhidrazona (FA-DNPH), apresenta maior estabilidade e proporciona boa sensibilidade na detecção, com absorbância ótima no comprimento de onda de 360 nm, considerando a intensidade e seletividade verificadas na matriz estudada.
Assim, o preparo de amostra foi realizado pesando-se 4,5 g de leite em tubo cônico de polipropileno de 15 mL, ao qual foram adicionados 0,5 mL da solução de DNPH acidificada com ácido fosfórico (pH = 3,0) e 5,0 mL de acetonitrila. Após agitação em vórtice durante 30 s, os tubos foram centrifugados a 3600 rpm por 5 min. O sobrenadante resultante foi transferido para um balão de 10 mL, lavando-se o tubo com FM, e completando o volume do balão com a mesma mistura de solventes. A solução obtida foi filtrada com filtros de seringa de PTFE com poros de 0,45 μm para vials de 2 mL e analisada por CLAE-DAD. As etapas do preparo encontram-se descritas na figura 1b.
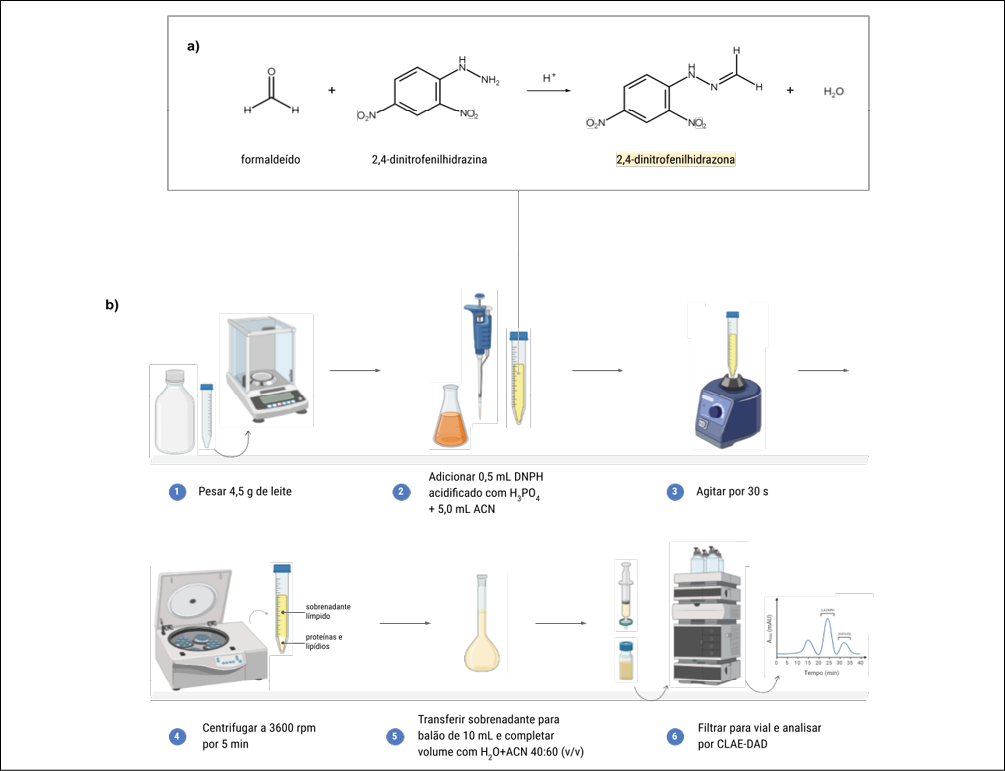
Figura 1 – (a) Reação entre formaldeído e 2,4-dinitrohidrazina em meio ácido, formando 2,4-dinitrofenilhidrazona com eliminação de água. (b) Etapas do preparo das amostras de leite, compreendendo extração líquido-líquido com acetonitrila e derivatização com DNPH.
2.4 ANÁLISE
Um cromatógrafo 1200 Series da Agilent Technologies (Santa Clara, EUA) foi utilizado para a realização das análises. A separação cromatográfica foi conduzida em uma coluna Zorbax Eclipse Plus C18 de 150 mm x 4,6 mm de diâmetro interno, com tamanho de partícula 5 μm também da Agilent, mantida à temperatura ambiente. Para o estudo de robustez, também foi utilizada a coluna Agilent Zorbax Eclipse XDB C18 150 × 4,6 mm, 5 μm. A fase móvel consistiu de uma mistura isocrática de água e acetonitrila na proporção 40:60 (v/v) a um fluxo de 1 mL/min. O volume de injeção foi de 20 μL, com tempo total de corrida de 5 minutos. O comprimento de onda de 360 nm do detector DAD foi utilizado para quantificação do analito, e o controle do sistema e processamento dos dados foi realizado por meio do software Agilent ChemStation.
Após a otimização, o método foi validado segundo os procedimentos recomendados pelo INMETRO23 e pela Agência Nacional de Vigilância Sanitária (ANVISA)24, avaliando-se os parâmetros seletividade, efeito matriz, linearidade, exatidão, precisão (incluindo repetibilidade e precisão intermediária), limite de detecção (LD), limite de quantificação (LQ) e robustez.
A seletividade foi avaliada comparando-se os cromatogramas obtidos para a matriz fortificada com formaldeído, branco de amostra e branco dos reagentes. O efeito matriz foi estudado por meio da comparação entre curvas de calibração preparadas em solvente e em matriz.
Uma curva de calibração em matriz com cinco níveis de concentração, 0,03, 0,05, 0,06, 0,08 e 0,10 mg/L, foi preparada em triplicata para demonstração da linearidade. No caso da exatidão, foram fortificadas em triplicata amostras em três níveis de concentração, 0,03, 0,06 e 0,10 mg/L. Para a precisão, a repetibilidade foi avaliada pela análise de seis réplicas de amostra fortificada a 0,06 mg/L em um mesmo dia, e a precisão intermediária (interdia) com seis réplicas na mesma concentração analisadas em dois dias diferentes e com analistas diferentes.
O LD e o LQ foram estimados a partir dos parâmetros da curva de calibração, calculando-se seus valores, respectivamente, como a razão entre 3 e 10 vezes o desvio padrão do coeficiente linear (σ) e o valor médio do coeficiente angular (a) obtidos das três curvas de calibração preparadas na matriz, ou seja, e .
Por fim, a robustez foi avaliada comparando-se a recuperação do analito adicionado na concentração de 0,10 mg/L ao submeter as amostras a variações no pH (de 6,0 para 5,8 e 6,2), na composição (de proporção 40:60 entre H2O e ACN para 38:62 e 42:58), e no fluxo (de 1 para 0,8 e 1,2 mL/min) da FM, e na temperatura (de 25ºC para 20ºC e 30ºC), e tipo da coluna utilizadas na análise.
3 RESULTADO E DISCUSSÃO
A princípio, o desenvolvimento do método deste trabalho foi realizado através de uma otimização do método descrito por Kaminski et al.25. Tendo em vista que o método de extração e a quantificação do teor de DNPH-FA proposto no artigo referenciado mostrava-se moroso e complexo. O fator crucial para o desenvolvimento do método de extração foi a presença de grande quantidade de interferentes no leite, pois é constituído por proteínas e lipídios.
Através de testes para eliminação dos interferentes, a extração líquido-líquido com adição de 5 mL de acetonitrila (ACN), juntamente com a derivatização utilizando 0,5 mL da solução de DNPH acidificada com ácido fosfórico 85%, modificando o pH da solução para 3 e a posterior centrifugação do extrato foi que apresentou melhor resultado para precipitação das proteínas e lipídios contidos no leite, resultando em extratos mais limpos e livres de interferentes (Figura 1) que poderiam coeluir com o analito de interesse.
Conceitualmente, a partir desse princípio, o novo método de técnica analítico desenvolvido através da extração liquido-liquido empregando ACN e DNPH acidificado apresentou bons resultados, conforme Rezende et al.26, a formação da hidrazona desejada (FA-DNPH) é lenta em valores de pH muito baixos ou muito altos, sendo geralmente mais rápida na faixa de pH entre 4,0 e 5,0, sendo que a reação ótima ocorre em uma faixa de pH entre 3,0 e 4,5. Já no nosso caso o pH 3 foi que apresentou melhor resultado juntamente com a alteração da força do eluente na Fase Móvel composta de 40:60 (H2O:ACN) a um fluxo de 1 mL/min, tornando a separação adequada do DNPH-FA, com tempo de análise de 5 minutos, demonstrando ser um método menos complexo ao comparar com Kaminski et al.25 e Rezende et al.26 (comparação descrita na Tabela 1).
Tabela 1 – Comparação dos parâmetros de otimização de métodos de formaldeídos em leite pelo HPLC
|
Parâmetros |
Método Kaminski et al.25 |
Método Rezende et al.26 |
Método desenvolvido |
|
Comprimento de onda |
345 nm |
360 nm |
360 nm |
|
Fase estacionária |
C8 |
C18 |
C18 |
|
Fase móvel |
H2O/ACN – (60:40%) |
H2O/ACN – (35:65% por 6 min. (H2O/ACN – (10:90%) por 8 min. |
H2O/ACN – (40:60%) |
|
Tamanho da coluna |
250 x 4,6 mm; partícula de 10 µm |
250 × 4,6 mm partícula; 5 μm |
150 x 4,6 mm, partícula de 5 µm |
|
Detector |
UV-Vis |
UV-Vis |
DAD |
|
Preparo de amostra |
Extração liquido-liquido com hexano |
Extração liquido-liquido com DNPH/ACN particionamento a baixa temperatura (LLE-LTP) -4ºC |
Extração liquido-liquido com DNPH/ACN |
|
Tempo de Preparo de amostra |
≈ 50 min |
≈ 4 a 12 h devido ao resfriamento |
≈ 10 min |
|
Tempo de corrida |
28 min |
8 min |
5 min |
|
LQ |
0,09 mg/L |
0,02 mg/L |
0,01 mg/L |
|
Exatidão / Recuperação (0,1 mg/L) |
96,9 % |
102,2 % |
98 % |
A confiabilidade desses resultados analíticos gerada no trabalho está associada à validação do método. Tendo que a seletividade e a especificidade do método foram comprovadas, através do pico do analito de interesse (FA) na qual apresentou resolução > 1,5 e assimetria entre 0,80 e 1,20.
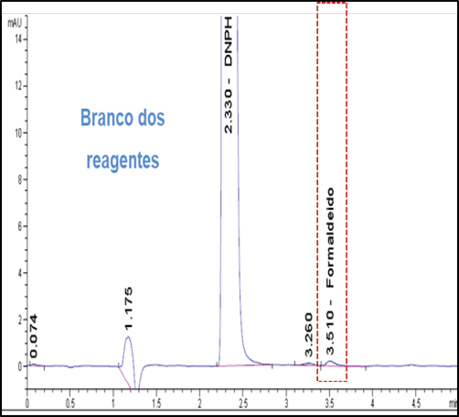
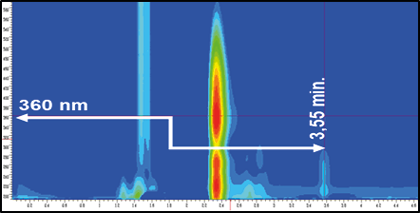
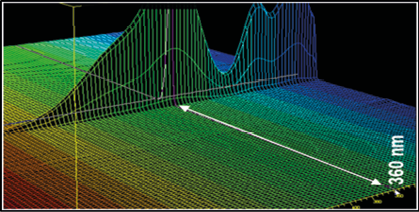
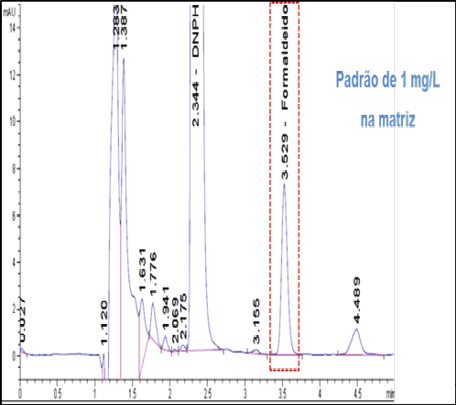
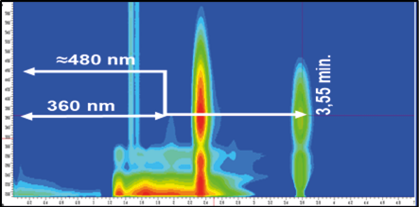
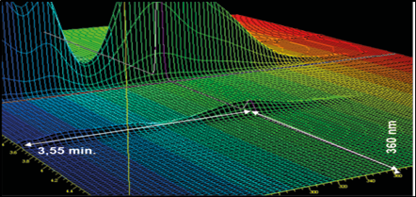
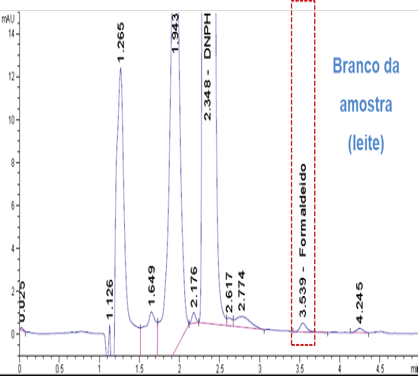
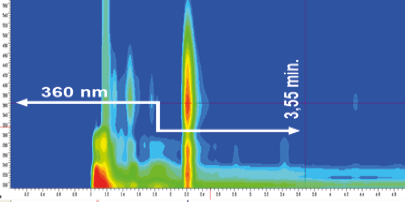
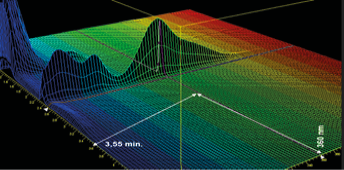
Ao observar os picos e os espectros de absorção em 2D e 3D nos cromatogramas de 2,4 - dinitrofenilhidrazona de formaldeído (DNPH-FA) (Figura 2), referentes ao branco dos reagentes, solução de leite com adição de 1 mg/L de FA e branco da amostra, fica claro que a pureza do pico no tempo de retenção de 3,55 min. do DNPH-FA foi garantida demonstrando que não houve coeluição do pico de interesse com os picos interferentes, evidenciando a seletividade do método.
O estudo de efeito matriz confirmou as interferências nas bandas de absorção exercendo um efeito negativo (-14%), ou seja, houve um decréscimo de sinal sobre o resultado das análises que segundo estabelecido pelo documento de validação do NATA27 considera que a diferença não é significativa se estiver abaixo de 10%, assim a curva analítica foi preparada na matriz (leite) para minimizar e corrigir este efeito.
Ao analisar o estudo matemático através das relações estatísticas do parâmetro de linearidade para DNPH-FA por CLAE-DAD, apresentou resultado satisfatório, por meio do coeficiente de correlação (r2) > 0,99 indicando um bom ajuste do modelo linear. Os dados da análise de regressão linear estão demonstrados na Tabela 2 e na (Figura 3).
Tabela 2 – Análise de regressão linear para quantificação de DNPH-FA em leite
|
Parâmetros da regressão |
Resultados obtidos |
|
Coeficiente de determinação (r2) |
0,998 |
|
Inclinação ± desvio padrão |
399 ± 0,8 |
|
Intercepto ± desvio padrão |
0,27 ± 0,01 |
|
Desvio padrão relativo (%) |
4,2 % |
|
Faixa de concentração (mg/L) |
0,03 – 0,10 |
|
Número de pontos |
5 |
|
H0: a = 0 |
Limite inferior: - 0,66 |
|
Limite superior: 0,59 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Figura 2 – Cromatogramas das análises de seletividade DNPH-FA, espectros de absorção em 2D e 3D. Nota: No cromatogramas, onde se lê formaldeído, lê-se 2,4 - dinitrofenilhidrazona de formaldeído (DNPH-FA).
Outro ponto importante a ser considerado na avaliação da linearidade é o teste de Hipótese zero (H0: a = 0 intercepto) onde o limite inferior e superior -0,66 e 0,59 passam bem próximo da origem (ponto zero da curva) o que denota que as concentrações de trabalho estão dentro da faixa linear e que os erros sistemáticos não são significativos ao nível de confiança de 95%.
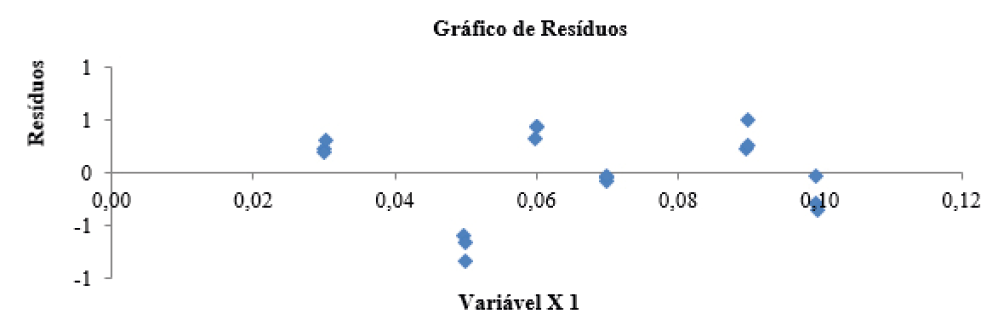
Na Figura 4, demonstra que há uma distribuição aleatória ao redor da linha de resíduo zero e os valores dos resíduos estão randomicamente distribuídos, evidenciando que o método não apresenta qualquer tendência e, portanto, apresenta linearidade adequada, conforme estabelecido pela Resolução ANVISA - RDC Nº 166 de 201724 – Guia para validação de métodos analíticos.
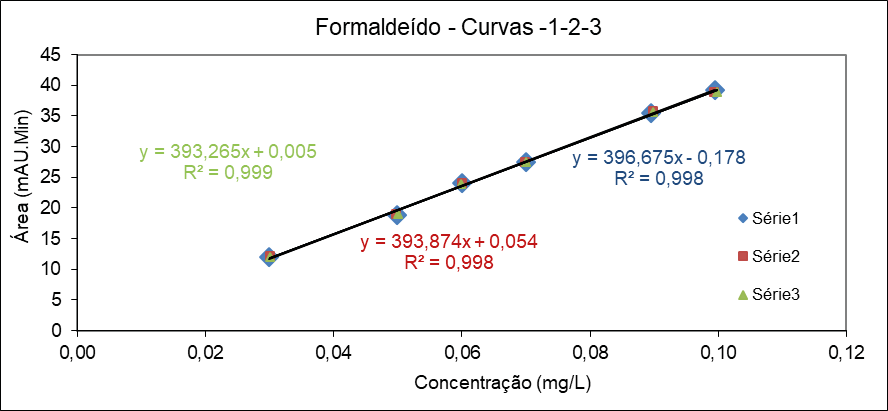
Figura 3 – Curvas de linearidade de DNPH-FA na faixa de 0,03 a 0,10 mg/L em leite

Figura 4 – Resíduos versus as concentrações de DNPH-FA adicionadas ao leite
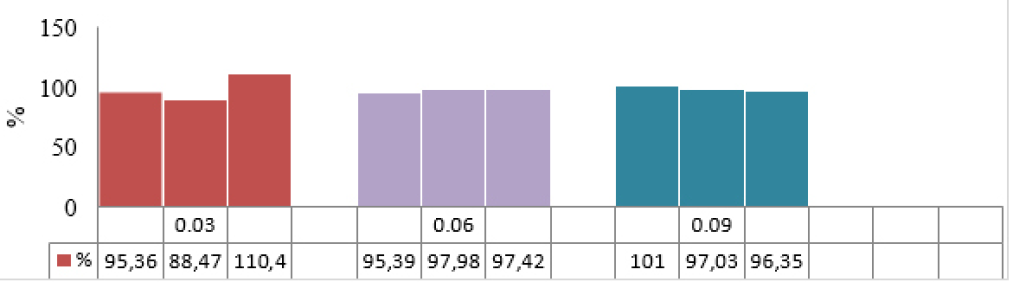
A precisão do método foi demonstrada a partir do Desvio Padrão Relativo (DPR) igual 2% obtido na análise de precisão intra-corrida e da precisão intermediária que apresentou Coeficiente de Variação (CV%) máxima de 4% para (n=6), com as adições independentes de FA 0,06 mg/L na matriz leite, com variações inferiores a 5%, o que comprova a repetibilidade e a reprodutibilidade do método na determinação DNPH-FA em leite com base na média dos resultados obtidos em diferentes dias de análise e por diferentes analistas. A exatidão do método foi confirmada através da percentagem de recuperação de DNPH-FA no método de adição de padrão em três diferentes faixas (0,03, 0,06 e 0,09 mg/L) e os resultados obtidos ficaram na faixa de 88% a 110% e DPR 6% abaixo de 10%, pois estes apresentaram níveis de recuperação aceitáveis indicando boa exatidão para o método de CLAE-DAD desenvolvido para a determinação de formaldeído em leite, considerando a complexidade dessa matriz, conforme Figura 5. É importante evidenciar que esses valores estão de acordo com os critérios estabelecidos pelo Codex Alimentarius28.
Os LD e LQ foram definidos respectivamente como 3 x s/b e 10 x s/b, onde s é o desvio padrão de 7 medidas do branco com adição de 0,03 mg/L de FA nas amostras e b é a inclinação da curva analítica obtida por regressão linear20-21.
Os valores obtidos para LD e LQ do método foram, respectivamente, 0,004 mg/kg e 0,01 mg/kg. O DPR entre as concentrações foi de 2% e a recuperação apresentou uma média de 112%, demonstrando que o LQ tem precisão e recuperação aceitáveis, ou seja, dentro dos critérios estabelecidos na literatura21.
A avaliação da robustez frente às variações de pH da FM, temperatura da coluna, composição da FM e diferentes colunas, demonstrou que o método é robusto, pois apresentaram DPR > 5%, inclusive em Rezende et al.26 também afirma não ter encontrado variação significativa de áreas de pico e tempo de retenção, apresentando eficácia para possíveis variações de uma rotina de análises, indicando o não comprometimento da sua confiabilidade, exceto para a variação do fluxo da FM que apresentou DPR 19,2% muito superior ao aceito 5%, principalmente para a diminuição do fluxo de 1 mL/min. para 0,8 mL/min, que comprometeu o tempo de retenção e a área do pico de DNPH-FA. Os resultados podem ser visualizados na Tabela 3.

Figura 5 – Porcentagem de recuperação nas concentrações baixa (0,03 mg/L), média (0,06 mg/L) e alta (0,09 mg/L) de FA adicionadas na amostra
Tabela 3 – Estudo de robustez do método
|
Parâmetros |
DPR (%) |
Recuperação (%) |
|
Fluxo da fase móvel (mL/min) |
19,2 |
104 |
|
Composição da fase móvel H2O: ACN |
3,5 |
101 |
|
Temperatura da coluna °C |
3,2 |
100 |
|
pH da fase móvel |
3,3 |
101 |
|
Coluna (fase estacionária) |
3,3 |
100 |
O método depois de validado foi aplicado para determinação de FA em quinze amostras de leite de tipos e marcas diferentes, comercializadas nos supermercados da cidade de São Paulo, sendo que apenas uma apresentou valor acima do LQ, onde a concentração encontrada de DNPH-FA foi de 0,028 mg/kg com recuperação de 93%, conforme Tabela 4.
Tabela 4 – Teor de DNPH-FA das quinze amostras de diferentes tipos de leite UHT
|
Amostras |
Concentração de FA nas amostras (mg/kg) |
Concentração adicionada de FA na amostra (mg/kg) |
Recuperação (%) |
|
Leite integral (A) |
0,028 |
0,04 |
93 |
|
Leite integral (B) |
LQM < 0,01 |
0,03 |
104 |
|
Leite integral (C) |
LQM < 0,01 |
0,03 |
93 |
|
Leite integral (D) |
LQM < 0,01 |
0,03 |
70 |
|
Leite integral (E) |
LQM < 0,01 |
0,10 |
100 |
|
Leite semi-desnatado (A) |
LQM < 0,01 |
0,04 |
78 |
|
Leite semi-desnatado (B) |
LQM < 0,01 |
0,05 |
86 |
|
Leite semi-desnatado (C) |
LQM < 0,01 |
0,05 |
97 |
|
Leite semi-desnatado (D) |
LQM < 0,01 |
0,05 |
103 |
|
Leite desnatado (A) |
LQM < 0,01 |
0,06 |
91 |
|
Leite desnatado (B) |
LQM < 0,01 |
0,06 |
87 |
|
Leite desnatado (C) |
LQM < 0,01 |
0,06 |
79 |
|
Leite desnatado (D) |
LQM < 0,01 |
0,06 |
86 |
|
Leite sem lactose (A) |
LQM < 0,01 |
0,03 |
82 |
|
Leite sem lactose (C) |
LQM < 0,01 |
0,03 |
70 |
Apesar das demais amostras não apresentarem teor de FA acima do LQ, a recuperação para concentrações de 0,03 a 0,06 mg/kg de DNHP-FA demonstraram resultados acima de 70% com ótimos resultados de precisão e exatidão.
O estudo realizado por Rezende et al.26 teve como objetivo quantificar o teor de formaldeído através da extração líquido-líquido com particionamento a baixa temperatura (LLE-LTP) e detecção por CLAE-UV em 13 amostras de diferentes tipos de leite bovino. Das 13 amostras analisadas, 38,5 % apresentavam teor de formaldeído entre 0,026 a 0,055 mg/kg. Sendo que duas amostras eram de leite integral UHT (0,026 e 0,055 mg/kg), uma de leite em pó desnatado (0,028 mg/kg) e duas amostras de leite em pó integral (0,035 e 0,046 mg/kg).
4 CONCLUSÕES
Finalmente, podemos concluir que o método desenvolvido e validado neste estudo é bastante sensível se comparado com o método oficial, de modo que é obtido uma quantificação do (FA) de LDM e LQM 0,004 mg/kg e 0,01 mg/kg respetivamente. Apresentando um ótimo resultado de exatidão na faixa de 88% a 110% de recuperação. E a sua precisão apresentou coeficiente de variação (CV) na faixa de 1% a 4% demonstrando ser seletivo, preciso e exato.
Um dado relevante é que este método atualmente empregado confere a contaminação de FA no leite através da comparação com uma solução padrão de 1 mg/L de FA, de forma não seletiva, pois não faz distinção da presença de FA de origem endógena ou fraudulenta, quando a faixa de concentração baixa é encontrada no leite. Desta forma, o método aqui desenvolvido pode colaborar para o aumento de segurança alimentar, beneficiando diretamente a sociedade de consumo.
Testes futuros propõem a realização do método aqui apresentado em amostras de leite em pó para lactentes e de crianças de primeira infância, a fim de detectar se há contaminação de traços de FA nestes produtos, assim como, falhas no controle de qualidade das indústrias de alimentos e no processo de fiscalização, uma vez que o consumo deste tipo de alimento passou a aumentar, pois hoje muitos bebês e crianças pequenas dependem desta fórmula infantil como sua principal fonte de nutrição.
AGRADECIMENTOS
Ao Instituto de Pesquisas Tecnológicas do Estado de São Paulo - IPT na figura de Sandra Souza de Oliveira, por conceder a infraestrutura e a oportunidade de desenvolver tal pesquisa. Prof. Dr. Adriano Marim, de Oliveira, Dra. Carolina Fracalossi Rediguieri e a Dra. Camila Areias de Oliveira por sugestões e colaboração.
REFERÊNCIAS
- Behmer MA. Tecnologia do leite. São Paulo: Nobel; 1999.
- Universidade de São Paulo. Tabela Brasileira de Composição de Alimentos (TBCA). Food Research Center (FoRC). Versão 7.1. São Paulo; 2020 [citado em 2022 Ago 12]. Disponível em: http://www.fcf.usp.br/tbca
- Instituto Brasileiro de Geografia e Estatísticas. Quantidade de leite cru adquirido e industrializado e variação, segundo os meses. Brasil; 2022 [citado em 2023 Maio 20]. Disponível em: https://www.ibge.gov.br/estatisticas/economicas/agricultura-e-pecuaria/9209-pesquisa-trimestral-do-leite.html?edicao=36443&t=resultados
- Companhia Nacional de Abastecimento. Análise Mensal. Leite e Derivados. 2023 Mar [citado em 2023 Maio 23]. Disponível em: https://www.conab.gov.br/info-agro/analises-do-mercado-agropecuario-e-extrativista/analises-do-mercado/historico-mensal-de-leite
- Nascimento CF, Santos PM, Pereira-Filho ER, Rocha FRP. Recent advances on determination of milk adulterants. Food chemistry. 2017;221:1232-44.
- Agência Nacional de Vigilância Sanitária. Relatório Estatístico. 2013 Abr [citado em 2023 Maio 23]. Disponível em: http://portal.anvisa.gov.br/documents/111522/2781944/Relat%C3%B3rio+Estat%C3%ADstico+Abril+2013/931ca621-8eb5-4819-b165-eb7a98766368
- Instituto Nacional de Câncer. Formol. 2022 [citado em 2023 maio 1]. Disponível em: https://www.gov.br/inca/pt-br/assuntos/causas-e-prevencao-do-cancer/exposicao-no-trabalho-e-no-ambiente/solventes/formol
- Costa ALR. Incidência de fraudes, alterações e adulterações em leite cru refrigerado comercializado clandestinamente no norte do Tocantins. [Trabalho de Conclusão de Curso]. Araguaína, TO: Universidade Federal do Norte do Tocantins; 2021 [citado em 2023 Maio 4]. Disponível em: http://repositorio.uft.edu.br/handle/11612/3066
- Huaixiang T, Wu D, Chen B, Yuan H, Yu H, Lou X, et al. Rapid identification and quantification of vegetable oil adulteration in raw milk using a flash gas chromatography electronic nose combined with machine learning. Food Control. 2023;150:109758.
- Guerreiro TM, Oliveira DN, Melo CFOR, Oliveira Lima E, Ribeiro MDS, Catharino RR. Evaluating the effects of the adulterants in milk using direct-infusion high-resolution mass spectrometry. Food Res Int. 2018;108:498-504.
- Oliveira SRB, Moraes LDS, Coelho CP. Fraudes em alimentos industrializados. Pubsaúde. 2021;5:115. doi: https://dx.doi.org/10.31533/pubsaude5.a115
- Balan B, Dhaulaniya AS, Jamwal R, Amit, Sodhi KK, Kelly S, et al. Application of Attenuated Total Reflectance-Fourier Transform Infrared (ATR-FTIR) spectroscopy coupled with chemometrics for detection and quantification of formalin in cow milk. Vibrational Spectroscopy. 2020;107:103033.
- European Food Safety Authority. Endogenous formaldehyde turnover in humans compared with exogenous contribution from food sources. EFSA Journal. 2014;12(2):3550. doi: https://doi.org/10.2903/j.efsa.2014.3550
- Brasil. Ministério da Justiça, Ministério da Agricultura, Pecuária e Abastecimento, “Instrução Normativa nº 68, de 12 de dezembro de 2006”. Diário Oficial da República Federativa do Brasil. 2006 Dez 14;(seção 1):8-32.
- Association of Official Analytical Chemists. AOAC. Official Method 931.08 Formaldehyde in Food.
- Khalil SR, Awad A, Ali SA. Melamine and/or formaldehyde exposures affect steroidogenesis via alteration of StAR protein and testosterone synthetic enzyme expression in male mice. Environmental toxicology and pharmacology. 2017;50:36-144.
- Wanderley CH, Silva ACO, Silva FER, Mársico ETM, Conte Junior CA. Avaliação da sensibilidade de métodos analíticos para verificar fraude em leite fluido. Revista de Ciências da Vida. 2013;33(1/2):54-63.
- Faria IDL, Gouvêa MM, Netto ADP, Marques FFC. Determination of formaldehyde in bovine milk by micellar electrokinetic chromatography with diode array detection. LWT – Food Science and Technology. 2022:163:113473.
- Kochetkova M, Timofeeva I, Bulatov A. A derivatization and microextraction procedure with organic phase solidification on a paper template:Spectrofluorometric determination of formaldehyde in milk. Spectrochimica Acta, Part A:Molecular and Biomolecular Spectroscopy (SAA). 2021;263:120160.
- Giokas DL, Tsogas GZ, Vlessidis AG. On-line derivatization coupled to flow injection permanganate chemiluminescence detection of total carbonyl compounds in natural waters and drinking water. Analytica Chimica Acta. 2009;651(2):188-95.
- Pillai AKKV, Gautam K, Jain A, Verma KK. Headspace in-drop derivatization of carbonyl compounds for their analysis by high-performance liquid chromatography-diode array detection. Analytica Chimica Acta. 2009;632:208-15. doi: http://doi.org/10.1016/j.aca.2008.11.021
- Vairavamurthy A, Roberts JM, Newman L. Methods for determination of low molecular weight carbonyl compounds in the atmosphere:a review. Atmos. Environ. Part A, Gen. Top. 1992;26(11):1965-93.
- Instituto Nacional de Metrologia. DOQ-CGCRE-008:2016 Orientação sobre Validação de Métodos Analíticos. Revisão 05; 2011.
- Agência Nacional de Vigilância Sanitária. 2017 [citado em 2023 Maio 23]. Disponível em: http://portal.anvisa.gov.br/documents/10181/2721567/RDC166_2017_COMP.pdf/d5fb92b3-6c6b-4130-8670-4e3263763401
- Kaminski J, Atwal AS, Mahadevan S. High Performance Liquid Chromatographic Determination of Formaldehyde in Milk. Journal of Liquid Chromatography. 1993;16 (2):521-26, doi: https://dor.org/10.1080/10826079308020929
- Rezende FBF, Cheibub AMSS, Netto ADP, Marques FFC. Determination of formaldehyde in bovine milk using a high sensitivity HPLC-UV method. Microchemical Journal. 2017;134:383-89.
- National Association of Testing Authorities. Guidelines for the validation and verification of quantitative and qualitative test methods. Technical Note 17. Australia; 2013.
- Codex Alimentarius Comission. Guidelines for the design and implementation 75 of national regulatory food safety assurance programme associated with the use of veterinary drugs in food producing animals. GL, 2009;71:16. (Revised in 2012).
* Mestre em Processos Industriais no Instituto de Pesquisas Tecnológicas do Estado de São Paulo.
† Doutora em Medicamentos e Cosméticos pela Faculdade de Ciências Farmacêuticas de Ribeirão Preto da Universidade de São Paulo, Bionanomanufatura – Administração Bionano-IPT.
‡ Mestre em Processos Industriais com ênfase em Desenvolvimento e Otimização de Processos Industriais. Laboratório de Químicas Manufaturados – LQM-IPT.
§ Mestre em Tecnologia Nuclear - TNA pelo Instituto de Pesquisas Energéticas e Nucleares, IPEN-CNEN/SP., Brasil.
¶ Graduada em Farmácia-Bioquímica pela Faculdade de Ciências Farmacêuticas da Universidade de São Paulo; Laboratório de Químicas Manufaturados – LQM-IPT.
** Graduando em Engenharia Química na Universidade de Mogi das Cruzes (UMC). Laboratório de Químicas Manufaturados – LQM-IPT.
†† Graduada em Engenharia Química – Faculdades Osvaldo Cruz; Laboratório de Químicas Manufaturados – LQM-IPT.